MANUAL CADIFA DE PROCEDIMENTO ADMINISTRATIVOS Nº 01 (1ª Versão)
 (pdf)
(pdf)
SUMÁRIO
4.1 Módulo 1: Informações Administrativas
4.2 Módulo 2: Resumo Geral da Qualidade
IV. SISTEMAS DE PETICIONAMENTO
ANEXO 1: COMO ACESSAR O SISTEMA DE SUBMISSÃO
ANEXO 2: PETIÇÃO PRIMÁRIA (PROTOCOLO MANUAL)
ANEXO 3: PETIÇÃO PRIMÁRIA (PROTOCOLO ELETRÔNICO)
ANEXO 4: PETIÇÃO DE MUDANÇAS E OUTRAS (PROTOCOLO MANUAL)
ANEXO 5: PETIÇÃO DE MUDANÇA E OUTRAS (PROTOCOLO ELETRÔNICO)
ANEXO 6: CONTINUAÇÃO DE PETIÇÃO NÃO CONCLUÍDA
ANEXO 7: REIMPRESSÃO DE COMPROVANTE DE PROTOCOLIZAÇÃO
ANEXO 8: COMO ACESSAR O SOLICITA
ANEXO 9: PROTOCOLO DE CUMPRIMENTO DE EXIGÊNCIA
ANEXO 10: ACESSANDO CAIXA POSTAL E LENDO MENSAGEM
I. INTRODUÇÃO
CADIFA (carta de adequação de dossiê de insumo farmacêutico ativo) é o instrumento administrativo que atesta a adequação do DIFA (dossiê de insumo farmacêutico ativo) à Resolução – RDC nº 359/2020. Em outras palavras, atesta que a qualidade do IFA (insumo farmacêutico ativo) é adequadamente controlada pelo conjunto de testes que compõem sua especificação. A CADIFA não substitui o certificado de análise nem garante que um lote do IFA atenda as especificações.
A avaliação do DIFA não tem como objetivo verificar o cumprimento das boas práticas de fabricação (BPF), embora o fabricante tenha que assegurar que o IFA é produzido conforme os requerimentos de BPF. Assim, a CADIFA não é equivalente ao CBPF (certificado de boas práticas de fabricação) nem o substitui.
A CADIFA e o CBPF de IFA válidos são necessários para o deferimento do registro ou pós-registro de medicamento associado. Neste Manual, registro e pós-registro de medicamento, quando citados, serão sempre nos termos da Resolução – RDC 200/2017 e Resolução – RDC 73/2016, respectivamente. O solicitante/detentor do registro do medicamento é responsável pela qualidade do IFA utilizado na fabricação do medicamento.
Para se obter a CADIFA, o DIFA deve ser submetido na Anvisa pelo detentor do DIFA. A solicitação de CADIFA deve ocorrer de forma prévia e associada à petição de registro ou pós-registro de medicamento. Para ter CADIFA associada, o detentor do DIFA deve fornecer (1) carta ao solicitante/detentor do registro de medicamento, como número de referência do DIFA, autorizando o uso do seu DIFA como parte da análise da petição de registro ou pós-registro do medicamento; ou (2) cópia da CADIFA com a declaração de acesso preenchida, pelo detentor do DIFA, em nome do solicitante/detentor de registro do medicamento, quando o IFA já tem CADIFA.
Adicionalmente, a seu critério, a Anvisa poderá demandar a solicitação de CADIFA não associada a registro ou pós-registro de medicamento, após o deferimento de uma Manifestação de Interesse ou por convite público da Dicol (Diretorial Colegiada).
Por ausência de previsão legal, as petições relacionadas a CADIFA estão dispensadas do pagamento de Taxa de Fiscalização de Vigilância Sanitária (TFVS).
A estrutura e o conteúdo do DIFA foram propostos utilizando-se como base o CTD (documento técnico comum), disposto no GUIA nº 24 e seus Anexos. Este documento fornece orientações adicionais sobre a organização da informação no DIFA e de como submetê-lo na Anvisa em peticionamentos relacionadas a CADIFA. Aborda, também, como será a comunicação da Anvisa com o detentor do DIFA.
As informações e requerimentos descritos neste documento têm o objetivo de facilitar o fluxo e análise das petições relacionadas a CADIFA. Se necessário, de forma a possibilitar uma melhor apresentação, pode-se alterar o formato das informações, para facilitar o seu entendimento e avaliação dos resultados.
A submissão poderá ser manual (mídia eletrônica) ou eletrônica. A Anvisa sugere o peticionamento eletrônico do DIFA. Caso haja algum problema que já não seja tratado neste Manual, o detentor do DIFA poderá entrar em contato com a Anvisa pelo e-mail api@anvisa.gov.br com o assunto [Manual CADIFA].
II. ESCOPO
Este Manual é aplicável a todos os peticionamentos relacionados a CADIFA, bem como às comunicações entre o detentor do DIFA e a Anvisa.
III. ANTES DA SUBMISSÃO
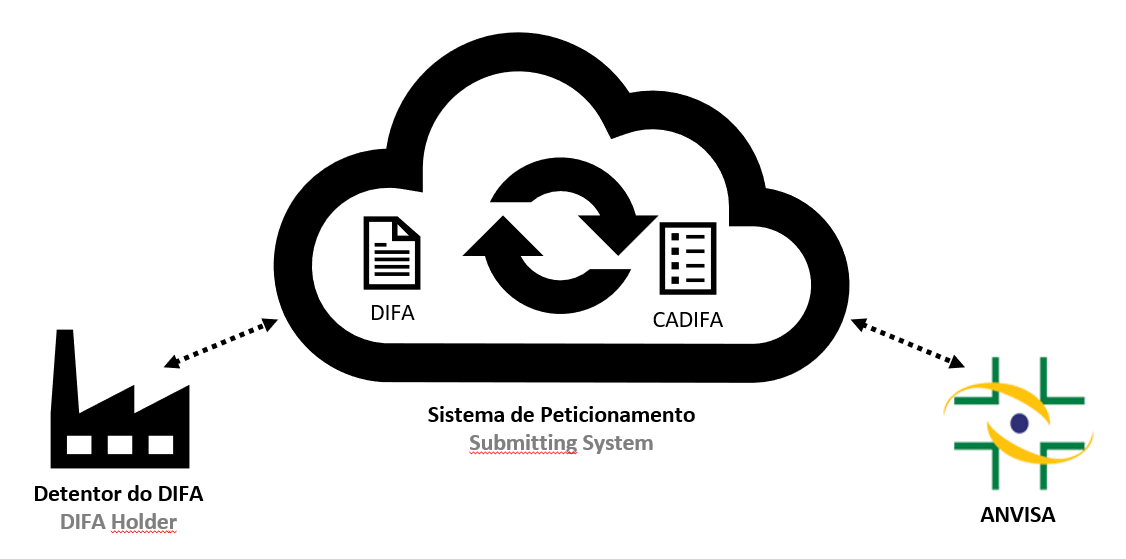
Os peticionamentos e as comunicações relacionados a CADIFA serão efetuados por meio de sistemas fornecidos pela Anvisa. Eles serão a interface entre o detentor do DIFA e a Agência para a transferência de informações regulatórias. Neles o detentor do DIFA submeterá informações à Anvisa e receberá informações dela de forma segura.
Previamente ao acesso aos sistemas da Anvisa, o detentor do DIFA deve, cadastrar-se, escolher o tipo de petição e organizar a documentação.

1. CADASTRO
O cadastro consiste em registrar o detentor de DIFA para fins de acesso aos sistemas da Anvisa (para mais informações sobre Cadastramento, acesse aqui). Nessa etapa o detentor do DIFA deverá indicar o seu gestor de segurança (para mais informações sobre Gestor de Segurança, acesse aqui).
De acordo com a Resolução – RDC nº 359/2020, detentor do DIFA é a “empresa que detém o conhecimento de todo o processo de fabricação do Insumo Farmacêutico Ativo (IFA) e sob cuja responsabilidade é realizada a fabricação do IFA, desde a introdução do material de partida”. Preferencialmente, o detentor do DIFA é o fabricante do IFA. Excepcionalmente, o(s) fabricante(s) podem se fazer representado(s) por outra empresa autorizada que será o detentor do DIFA. Não é aceita a submissão de documentação por terceiros que não o detentor do DIFA.
O Gestor de Segurança é a pessoa que atuará em nome do detentor do DIFA nos sistemas da Anvisa. Ele deve ser nomeado pelo responsável legal do detentor do DIFA e terá acesso a todas as informações peticionadas por ele, bem como a todas as informações emitidas pela Anvisa, inclusive aquelas confidenciais. Não há um número limite para Gestores de Segurança, recomendando-se pelo menos dois.
Como cadastrar?
O procedimento para cadastro dependerá se o detentor do DIFA (ou empresa representante) é domiciliado no Brasil e possui inscrição no Cadastro Nacional da Pessoa Jurídica (CNPJ).
- Caso a empresa possua CNPJ, o cadastro é feito em Cadastramento de Empresa; ou
- Caso a empresa não possua CNPJ, deve-se preencher o Formulário de Cadastro, assinar e enviar para o e-mail difa.holder@anvisa.gov.br. Após o cadastro será fornecido Número do Detentor do DIFA (DHN) e Número do Gestor de Segurança (AUN).
É de extrema importância que as informações do gestor de segurança estejam atualizadas. As comunicações da Anvisa com o detentor do DIFA ocorrerão por meio dele. O não recebimento das informações provenientes da Anvisa pode determinar o indeferimento de um peticionamento.
A alteração do cadastro deve seguir o mesmo procedimento acima, independentemente da necessidade do peticionamento de uma mudança do DIFA (mudanças administrativas do Anexo II da Resolução – RDC nº 359/2020).
2. TIPO DE PETIÇÃO
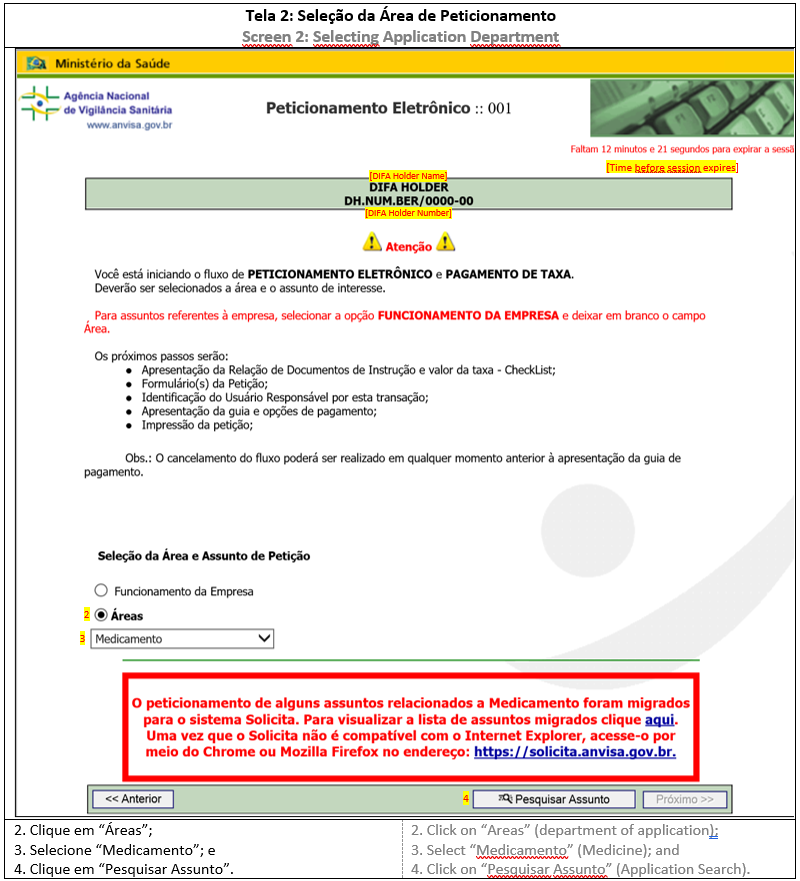
Antes de acessar o Sistema de Peticionamento, deve-se definir o assunto na Lista de Petições Relacionadas a CADIFA, já que ele determina o desenvolvimento da solicitação e os documentos que deverão ser apensados. Todas as petições são da área Medicamento e possuem um código, uma descrição de assunto e uma lista de verificação.
Todo peticionamento dará origem a um Número de Expediente. Adicionalmente, quando petição primária, a um Número de Referência (número do processo).
2.1 Petição Primária
A solicitação inicial (petição primária) poderá ser realizada por um dos três assuntos disponíveis: Solicitação de CADIFA Associada, Manifestação de Interesse ou Solicitação de CADIFA Não Associada. A ela será dado um número de referência (número do processo).
- A Solicitação de CADIFA Associada deve ser peticionada quando a CADIFA for necessária para a petição de registro ou pós-registro de medicamento. Nesse caso, o número de referência (número do processo) deverá ser enviado ao solicitante/detentor de registro do medicamento. Caso o número de referência não seja informado na petição de registro ou pós-registro de medicamento, a Solicitação de CADIFA Associada não será analisada e será encerrada;
- A Manifestação de Interesse deve ser peticionada quando o detentor do DIFA tiver interesse em obter uma CADIFA e não houver essa demanda por um solicitante/detentor de registro do medicamento. Nesse momento, só há o envio do Formulário de Petição; e
- A Solicitação de CADIFA Não Associada deve ser peticionada quando demandado pela Anvisa, após deferimento da Manifestação de Interesse ou por convite público da Diretoria Colegiada (Dicol).
Neste Manual, quando se mencionar Solicitação de CADIFA, ela irá se referir a Solicitação de CADIFA Associada e Solicitação de CADIFA Não Associada.
| Tipo de Peticionamento | Quando solicitar | |
|---|---|---|
| 1 | Solicitação de CADIFA Associada | Obtenção de CADIFA para utilização na petição de registro ou pós-registro de medicamento |
| 2 | Manifestação de Interesse | CADIFA não necessária para petição de registro ou pós-registro de medicamento |
| 3 | Solicitação de CADIFA Não Associada | Após deferimento de uma Manifestação de Interesse ou por convite público da Dicol |
DIFA Semelhante: Em alguns casos, o detentor do DIFA pode querer solicitar outra CADIFA para o mesmo IFA, seja porque não é possível solicitar uma mudança do DIFA ou porque ele quer CADIFAs separadas para condições diferentes de fabricação ou de qualidade (por exemplo, para cobrir um processo ou local de fabricação alternativo ou um outro grau de qualidade).
Para que o solicitante possa se beneficiar de uma análise mais rápida e harmonizada, o DIFA semelhante pode referenciar outro DIFA (aprovado ou aguardando análise), chamado aqui de DIFA original. Veja como evidenciar no Formulário de Petição.
Espera-se que algumas condições sejam atendidas em ambas solicitações:
- O nome e número DCB e número CAS sejam o mesmo;
- O IFA seja obtido da mesma forma (ex. extração vegetal, síntese química, fermentação clássica ou semissíntese);
- O detentor do DIFA seja o mesmo (ou do mesmo grupo); e
- O(s) fabricantes(s) seja(m) o(s) mesmo(s).
2.2 Petição de Mudança
Após a concessão da CADIFA e como parte do gerenciamento do ciclo de vida do DIFA, o detentor deve submeter a Petição de Mudança na Anvisa, conforme enquadramento das condições e acompanhada da documentação comprobatória descrita no Anexo II da Resolução – RDC nº 359/2020. A petição da mudança deve ser vinculada ao número de referência (número do processo) do DIFA.
Os códigos das mudanças estão dispostos na Lista de Petições Relacionadas a CADIFA. A manutenção do ciclo de vida do DIFA é condição primária para a manutenção da validade da CADIFA. A CADIFA NÃO POSSUI PROCEDIMENTO DE RENOVAÇÃO.
A mudança não prevista no Anexo II da Resolução – RDC nº 359/2020 será classificada como menor e deverá ser peticionada com o assunto “Menor por Exclusão”.
Mudanças Agrupadas:
O peticionamento de mudanças associadas ou decorrentes deve ser de forma conjunta, prevalecendo o enquadramento e tipo de implementação da mudança de maior risco.
Maior risco

|
Tipo de Mudança | Tipo de Implementação |
| Notificação Anual | Implementação Imediata | |
| Notificação Imediata | Implementação Imediata | |
| Menor | Após deferimento* | |
| Menor por Exclusão | Após Deferimento* | |
| Maior | Após Deferimento** | |
|
*Ou após 60 dias sem manifestação da Anvisa.
**Ou após 180 dias sem manifestação da Anvisa. |
||
Se mais de uma mudança for enquadrada na categoria de maior risco, orienta-se a escolha, nesta ordem de preferência, da petição da mudança que envolva: (1) controle de qualidade, (2) embalagem/cuidado de conservação/prazo de validade ou reteste, (3) fabricação e (4) protocolo de gerenciamento de mudança/design space.
A decisão da Anvisa será única para o conjunto das petições. Caso o detentor do DIFA opte pela implementação em separado das mudanças (por não serem decorrentes uma da outra), elas devem ser peticionadas separadamente. Por exemplo, a mudança de notificação anual ou notificação imediata peticionada em conjunto com uma mudança enquadrada como menor ou maior só poderá ser implementada após a manifestação favorável da Anvisa ou decurso do prazo previsto para análise.
A Anvisa sugere o peticionamento agrupado das mudanças de notificação anual que tenham sido implementadas dentro de 12 meses. Neste caso, o prazo para o peticionamento deve obedecer a data da implementação da primeira mudança e não no aniversário do produto. Quando uma das mudanças determinar a revisão da CADIFA (por exemplo mudanças 2.7.3 e 2.8.3), sugere-se a sua escolha para o peticionamento.
2.3 Cumprimento de Exigência
Durante a análise da Solicitação de CADIFA ou de uma Mudança, a Anvisa pode emitir uma Notificação de Exigência para solicitar informações ou esclarecimentos. O Cumprimento de Exigência deve ser peticionado em 120 (cento e vinte) dias, pelo detentor do DIFA, após leitura da Notificação de Exigência.
2.4 Outras Petições
À exceção do cumprimento de Exigência, após qualquer outro peticionamento, o detentor do DIFA pode submeter um Aditamento para complementação, não exigida formalmente, de informação já submetida e que não resulta em solicitação diversa da peticionada. O Aditamento será analisado em conjunto com a petição principal (indicado durante o peticionamento do Aditamento).
Ainda é possível peticionar a Desistência de qualquer petição, desde que a Anvisa não tenha tomado sua decisão.
É facultado ao detentor do DIFA peticionar a Suspensão (por até 2 anos) ou o Cancelamento da CADIFA.
O Recurso pode ser peticionado após o indeferimento de qualquer petição pela Anvisa. Nesse caso, devido a restrições legais, só é aceitável quando peticionado por um representante legal brasileiro. Adicionalmente, se o registro ou pós-registro do medicamento é indeferido (parcial ou integralmente) devido a informações referentes ao DIFA, o detentor do registro de medicamento pode peticionar o recurso no processo do medicamento associado e, se necessário, referenciando documentação técnica submetida no processo do DIFA.
3. TIPO DE PROTOCOLO
A Anvisa disponibilizará dois tipos de protocolo, manual e eletrônico, no Peticionamento eletrônico para os peticionamentos relacionados a CADIFA. O peticionamento das petições subsequentes deve ter a mesma forma de protocolo da petição primária, com exceção das petições disponíveis apenas no protocolo eletrônico.
O peticionamento com Protocolo Manual deverá ser no formato CTD, em suporte eletrônico (pen drive) e atender os requerimentos da seção “DO PROTOCOLO” do Guia 24/2019, versão 1. Esse tipo de protocolo terá a transação realizada no Peticionamento eletrônico e será concluído com a entrega da documentação em mídia eletrônica (pen drive) na Anvisa.
O peticionamento com Protocolo Eletrônico deverá atender ao disposto neste Manual e será iniciado e finalizado no Peticionamento eletrônico, com o envio da documentação pelo sistema e emissão de um comprovante de protocolo.
4. ORGANIZAÇÃO DO DIFA
O DIFA é composto por três módulos: Módulo 1 (Informação Administrativa), Módulo 2 (Resumo de Documentos Técnicos Comuns) e Módulo 3 (Qualidade). Para o protocolo eletrônico, os índices dos três módulos (seções 1.1, 2.1 e 3.1) e o Módulo 2 são opcionais.
A Anvisa sugere a adoção dos “Princípios Gerais”, “Granularidade”, “Paginação e Segregação de Documentos”, “Numeração de Seção em Documentos” e “Formatação de Índice” estabelecidos no GUIA nº 24, versão 1.
Requerimentos de Arquivo: Todos os arquivos devem ser submetidos em PDF (portable document format), permitirem cópia e busca textual e não podem exceder 60MB (megabytes) para os peticionamentos por protocolo manual e 20MB por protocolo eletrônico (arquivos maiores devem ser divididos). Recomenda-se que arquivos em PDF sejam gerados a partir de documentos eletrônicos (arquivos PDF digitalizados, normalmente, possuem qualidade inferior). Documentos digitalizados como imagem são mais difíceis de ler e não permitem procurar ou copiar e colar as informações. Deve-se evitar digitalização sempre que possível. Os arquivos não devem possuir configurações de segurança ou senhas protetoras. Campos de segurança devem ser configurados de forma a permitir impressão, edição, seleção de texto ou gráficos e adicionar ou alterar anotações aos campos do formulário.
Nome de Arquivo: A Anvisa sugere o uso dos nomes dispostos aqui. Esses nomes não são obrigatórios, mas recomendados, e podem ser complementados, reduzidos ou omitidos. Em algumas seções pode ser interessante o nome dos arquivos incluir o nome do procedimento analítico validado. Nos peticionamentos subsequentes devem-se utilizar os mesmos nomes dos arquivos da petição primária.
4.1. Módulo 1: Informações Administrativas
No Módulo 1, devem ser apresentados os documentos administrativos, requeridos na Resolução – RDC nº 359/2020 para o tipo de petição. O formato e a ordem do conteúdo a ser apresentado devem seguir o Anexo I do Guia 24/2019, versão 1 , adaptado abaixo para melhor entendimento.
Estrutura do Módulo 1, de acordo com o Anexo I do Guia 24/2019, versão 1.
1.1 Índice
Seguir as orientações do Anexo I do Guia 24/2019, versão 1. Essa seção é obrigatória apenas para os protocolos manuais.1.2 Informação Administrativa
1.2.1 Folha de rosto
Seguir as orientações do Anexo I do Guia 24/2019, versão 1. Essa seção é obrigatória apenas para os protocolos manuais.
1.2.2 Justificativa
Seguir as orientações do Anexo I do Guia 24/2019, versão 1. Essa infomração poderá ser incluída também no campo 1.1.2 do FP.
1.2.3 Fomulários de Petição
Seguir as orientações do Anexo I do Guia 24/2019, versão 1.
1.2.4 Cópia da Exigência Técnica
Seguir as orientações do Anexo I do Guia 24/2019, versão 1.
1.2.5 Comprovante de quitação da TFVS
Seguir as orientações do Anexo I do Guia 24/2019, versão 1.
[...]
1.3 Comunicações com a Agência
1.3.1 Atas de Reunião em Parlatório
Opcional, a não ser que, de outra forma, seja solicitado. Seguir as orientações do Anexo I do Guia 24/2019, versão 1.
1.3.2 Respostas recebidas via Central de Atendimento
Opcional, a não ser que, de outra forma, seja solicitado. Seguir as orientações do Anexo I do Guia 24/2019, versão 1.
1.3.3 Ofícios em resposta à questionamentos enviados a Agência
Opcional, a não ser que, de outra forma, seja solicitado. Seguir as orientações do Anexo I do Guia 24/2019, versão 1.
[...]
1.4 Outras Informações Administrativas
Opcional, a não ser que, de outra forma, seja solicitado. Seguir as orientações do Anexo I do Guia 24/2019, versão 1.[...]
1.6 Informações do Insumo Farmacêutico Ativo – IFA
[...]
1.6.5 Informações Regulatórias Internacionais
Opcional, a não ser que, de outra forma, seja solicitado. Seguir as orientações do Anexo I do Guia 24/2019, versão 1.
1.7 Petições Secundárias
[...]
1.7.4 Declarações Pós-Registro
Devem ser apresentadas a documentação solicitada no Anexo II da Resolução – RDC nº 359/2020, de acordo com a(s) mudança(s) peticionada(s).
[...]
Os documentos do Módulo 1 devem ser submetidos em PDF. A Anvisa disponibiliza modelos para folha de rosto, formulário de petição (FP) e declarações, que deverão ser assinados. O modelo de FP está estruturado de forma atender todos os tipos de peticão. Adicionalmente, sugere-se a submissão da Tabela Comparativa, quando necessária, em formato DOC/DOCX.
Complemento: No campo 1.2.1 do FP da submissão inicial, o detentor do IFA pode requerer um complemento de nome para o nome DCB do seu IFA a ser incluído na CADIFA (ex., tamanho de partícula, forma polimórfica, esterilidade, etc.). Ademais, ele é importante para diferenciar o DIFA Semelhante do DIFA original. Por exemplo, ele pode representar uma característica física do IFA (forma polimórfica II, etc.) ou um processo alternativo (processo 2, local X, código específico, etc.).
DIFA Semelhante: Sugere-se que o preenchimento do FP mencione que o peticionamento envolve a submissão de um DIFA Semelhante no campo 1.1.2, o DIFA original no campo 1.1.3 e o complemento no 1.2.1. A Tabela Comparativa (Anexo 9 do FP) com as diferenças entre os DIFAs é um documento determinante para a rapidez da análise.
Cumprimento de exigência: A não ser que solicitado, dispensa-se a submissão do FP no Cumprimento de exigência. No entanto, em seu lugar, deve-se submeter um ofício (apresentado na seção 1.2.4 do Módulo 1) listando as exigências e as respostas, com dados de suporte e, quando aplicável, referenciando as seções do DIFA atualizadas.
A critério do detentor do DIFA, outros documentos administrativos podem ser submetidos, obedecendo a estrutura do Módulo 1. Abaixo, segue um consolidado da documentação obrigatória, opcional ou não aplicável a ser apresentada, de acordo com o tipo de protocolo e de petição.
| Módulo 1 | Petições | ||||||
|---|---|---|---|---|---|---|---|
| Seção | Petição Primária | Mudança | Cumprimento de Exigência* | Outras* | |||
| 1.1 | Índice | (M) | O | ||||
| 1.2 | Informação Administrativa | 1.2.1 | Folha de Rosto | (M) | NA | ||
| 1.2.2 | Justificativa | O | NA | O | |||
| 1.2.3 | Formulário de Petição | (M)(E) | NA | (E) | |||
| 1.2.4 | Cópia da Exigência Técnica | NA | (E) | NA | |||
| 1.2.5 | Comprovante de quitação da TFVS | (M) | NA | ||||
| 1.2.6 | NA | ||||||
| 1.2.7 | |||||||
| 1.2.8 | |||||||
| 1.3 | Comunicações com a Agência | 1.3.1 | Atas de Reunião em Parlatório | O | |||
| 1.3.2 | Respostas recebidas via Central de Atendimento | ||||||
| 1.3.3 | Ofícios em resposta a questionamentos enviados a Agência | ||||||
| 1.3.4 | NA | ||||||
| 1.3.5 | |||||||
| 1.4 | Outras informações administrativas | O | |||||
| 1.5 | NA | ||||||
| 1.6 | Informações do IFA | 1.6.1 | NA | ||||
| 1.6.2 | |||||||
| 1.6.3 | |||||||
| 1.6.4 | |||||||
| 1.6.5 | Informações Regulatórias Internacionais | O | |||||
| 1.7 | Petições Secundárias | 1.7.1 | NA | ||||
| 1.7.2 | |||||||
| 1.7.3 | |||||||
| 1.7.4 | Declarações Pós-Registro | NA | (M)(E) | O | |||
| 1.7.5 | NA | ||||||
|
*Essas petições estarão disponíveis apenas no protocolo eletrônico.
Quando submeter? (M) – Obrigatório apenas no Protocolo Manual (E) – Obrigatório apenas no Protocolo Eletrônico (M) (E) – Obrigatório para os dois tipos de protocolo O – Opcional para os dois tipos de protocolo NA – Não se aplica para os dois tipos de protocolo |
|||||||
4.2. Módulo 2: Resumo Geral da Qualidade
O Módulo 2 é o resumo geral da qualidade que segue o escopo e estrutura do Módulo 3. Seu formato, organização e granularidade deve atender ao disposto no Anexo II do Guia 24/2019, versão 01. A sua submissão é obrigatória apenas na submissão inicial do DIFA pelo protocolo manual.
| Módulo 2 | Petições | ||||||
| Seção | Petição Primária | Mudança | Cumprimento de Exigência | Outras | |||
| 2.1 | Índice (Módulos 2-3) | (M) | NA | ||||
| 2.2 | Introdução | O | |||||
| 2.3 | Resumo Geral da Qualidade | 2.3.S | Insumo Farmacêutico Ativo | (M) | |||
|
Quando submeter?
(M) – Obrigatório apenas no Protocolo Manual O – Opcional para os dois tipos de protocolo; e NA – Não se aplica para os dois tipos de protocolo. |
|||||||
4.3 Módulo 3: Qualidade
O Módulo 3 contém os documentos com as informações sobre qualidade do IFA, conforme requisitado na Resolução – RDC nº 359/2020. Seu formato, organização e granularidade devem atender ao disposto no Anexo II do Guia 24/2019, versão 01 .
Quando houver restrição de confidencialidade entre o detentor do DIFA e o solicitante do registro do medicamento, a documentação de qualidade deve ser dividida em parte aberta e parte restrita, conforme Anexo III da Resolução – RDC nº 359/2020. A parte aberta deve conter informações suficientes para permitir ao solicitante/detentor do registro do medicamento avaliar a qualidade do IFA e sua adequabilidade para a fabricação do medicamento.
IV. SISTEMAS DE PETICIONAMENTO
Com exceção do peticionamento do cumprimento de exigência, a submissão de documentos nos peticionamentos relacionados a CADIFA utilizarão o Peticionamento Eletrônico. Para acessar o sistema, ver o ANEXO 1: COMO ACESSAR O SISTEMA DE SUBMISSÃO. A partir da tela principal é possível realizar as demais ações.
O sistema Solicita (mais informações sobre o sistemas estão disponíveis em seu Manual do Usuário, Versão 2.0) deve ser utilizado para:
- Recebimento e leitura de documentos provenientes da Anvisa (notificação de exigência, ofícios e CADIFA); e
- Protocolo do cumprimento de exigência.
| Sistemas de Peticionamento | ||
| Peticionamento Eletrônico | Sistema Solicita | |
| Atividade | Peticionamento | Cumprimento e Caixa Postal |
| Usuário e senha | Gestor de Segurança | |
| Navegador | Internet Explorer 11 | Chrome ou Mozilla Firefox |
Número de Transação: Independentemente do tipo de peticionamento e de protocolo, após a confirmação do tipo de petição, é gerado um número de transação que é enviado por mensagem automática pela Anvisa (sistemas@anvisa.gov.br) para o e-mail do gestor de segurança. Essa mensagem também é enviada ao final do peticionamento, para o e-mail da empresa e para o e-mail do gestor de segurança.

O número de transação permite a retomada do peticionamento da tela “Detalhes do Tipo de Petição” caso o sistema expire, ver ANEXO 6: CONTINUAÇÃO DE PETIÇÃO NÃO CONCLUÍDA. Se após a inserção do número de transação aparecer a mensagem da Figura 4, um novo peticionamento deve ser iniciado.
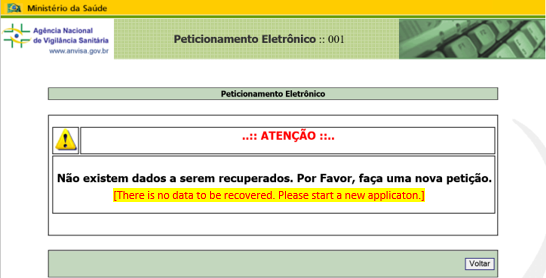
Lista de verificação: Cada tipo de petição possui um checklist específico com a documentação que deve ser anexada no peticionamento. Cada documento anexado deve ser visualizado antes de se prosseguir para a próxima etapa de peticionamento.
1. PROTOCOLO MANUAL
Esse tipo de protocolo será iniciado no Peticionamento eletrônico e concluído após o recebimento da documentação e mídia eletrônica (pen drive) na Anvisa, quando é dado o número de referência (número do processo) e de expediente.
Ao finalizar o procedimento no Peticionamento eletrônico, será emitido um comprovante da transação com o número de transação e o comprovante de isenção do pagamento de TFVS. Esses documentos deverão ser impressos e entregues na Anvisa junto com:
- Folha de rosto (impressa);
- Formulário de petição (impressa); e
- Mídia eletrônica (pen drive) em envelope lacrado identificado com nome da empresa, nome do IFA e número de transação. Para as petições secundárias, informar o número do processo.
|
À Agência Nacional de Vigilância Sanitária (Anvisa)
COIFA SIA Trecho 5, Área especial 57, Lote 200 CEP: 71205-050 Brasília – DF, Brasil |
Para peticionar uma Solicitação de CADIFA ou Manifestação de Interesse, ver o ANEXO 2: PETIÇÃO PRIMÁRIA (PROTOCOLO MANUAL). Atenção especial deve ser dada a granularidade escolhida, que irá determinar os arquivos que serão anexados. Essa granularidade deverá ser mantida nos peticionamentos subsequentes.
Para os peticionamentos subsequentes (com exceção do cumprimento de exigência), como Mudança ou Outros, ver o ANEXO 4: PETIÇÃO DE MUDANÇA E OUTRAS (PROTOCOLO MANUAL). A associação dessa petição ao processo da CADIFA será realizada pela Anvisa, após o recebimento da documentação e finalização da transação.
2. PROTOCOLO ELETRÔNICO
O peticionamento com Protocolo Eletrônico deverá atender ao disposto neste Manual. Ele será iniciado e finalizado no Peticionamento eletrônico, com o envio da documentação pelo sistema e emissão de um comprovante.
Comprovante de Protocolização On-Line: Após qualquer peticionamento com protocolo eletrônico é emitido um comprovante com as informações da petição, do gestor de segurança e do detentor do DIFA. Após a Solicitação de CADIFA, o número de referência (número do processo) deve ser informado ao solicitante/detentor de registro de medicamento para que possa ser utilizado no registro ou pós-registro de medicamento.

Caso necessário, pode-se reimprimir o comprovante, conforme ANEXO 7: REIMPRESSÃO DE COMPROVANTE DE PROTOCOLIZAÇÃO ON-LINE.
Para peticionar uma Solicitação de CADIFA ou Manifestação de Interesse, ver o ANEXO 3: PETIÇÃO PRIMÁRIA (PROTOCOLO ELETRÔNICO). Atenção especial deve ser dada a granularidade escolhida, que irá determinar os arquivos que serão anexados. Essa granularidade deverá ser mantida nos peticionamentos subsequentes.
Para os peticionamentos subsequentes (com exceção do cumprimento de exigência), como Mudança ou Outros, ver o ANEXO 5: PETIÇÃO DE MUDANÇA E OUTRAS (PROTOCOLO ELETRÔNICO).
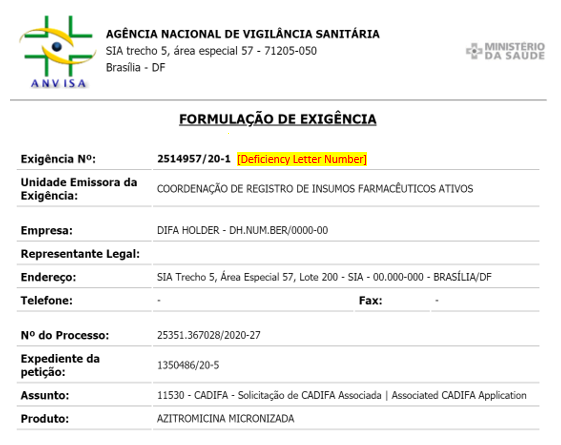
3. CUMPRIMENTO DE EXIGÊNCIA
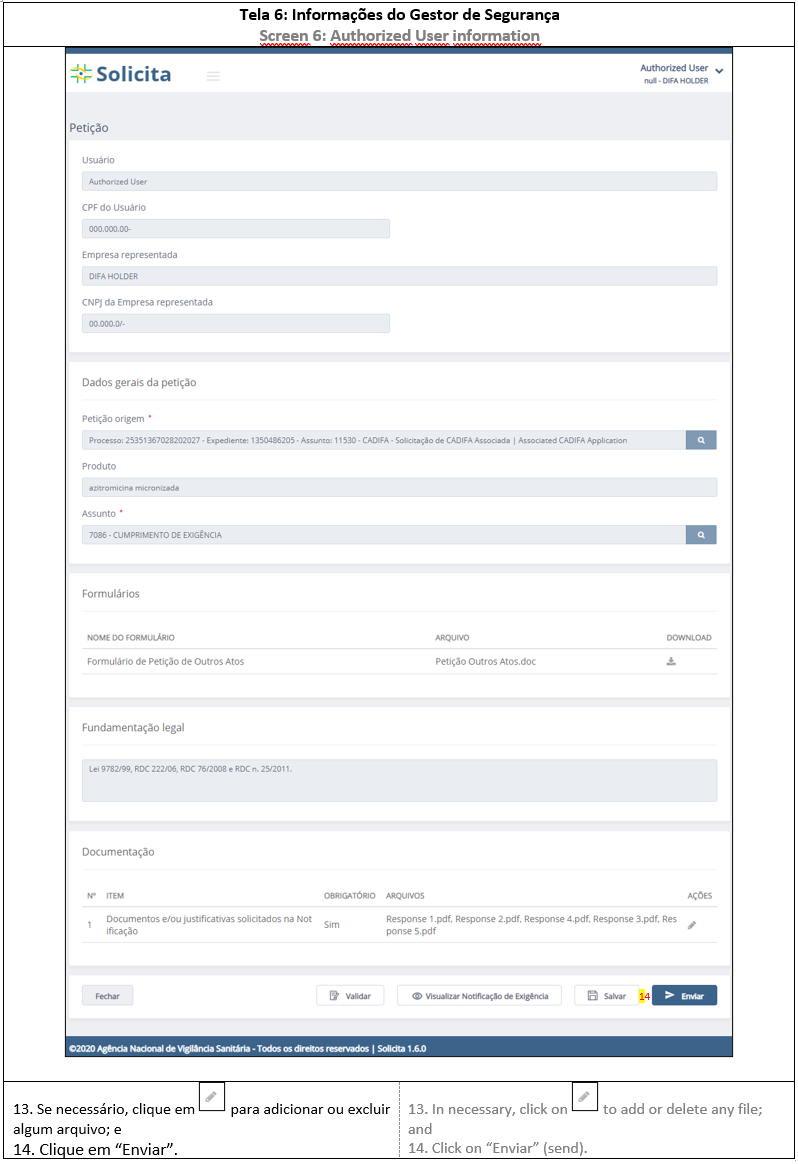
Para peticionar o Cumprimento de exigência, será necessário o número da notificação de exigência. Para a submissão ver ANEXO 9: PROTOCOLO DE CUMPRIMENTO DE EXIGÊNCIA.
4. CAIXA POSTAL
Após cada peticionamento ou a Anvisa enviar qualquer documento, ao acessar o sistema Solicita, o Gestor de Segurança será imediatamente notificado de que há nova mensagem não lida na Caixa Postal. Só será possível qualquer peticionamento após a leitura das mensagens não lidas.
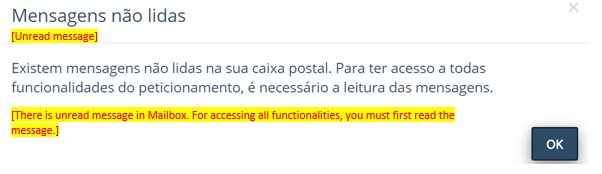
Para acessar a caixa postal e ler uma mensagem, ver ANEXO 10: ACESSANDO CAIXA POSTAL E LENDO MENSAGEM.
A Anvisa não enviará mensagens diretamente o e-mail do gestor de segurança sobre o envio de documentos para a Caixa Postal. Portanto, faz-se necessário o monitoramento constante da caixa postal para atendimento de notificações e recebimento de documentos da Anvisa.
V. APÓS A SUBMISSÃO
Os interessados podem acompanhar o andamento de qualquer petição, por meio do sistema de Consulta à Situação de Documentos, ver ANEXO 11: CONSULTA À SITUAÇÃO DE DOCUMENTOS. É possível cadastrar o e-mail para que seja notificado da situação do documento, semanalmente ou mensalmente, ver ANEXO 12: ACOMPANHANDO A SITUAÇÃO DE DOCUMENTOS.
Após a Solicitação de CADIFA, Petição de Mudança ou Cumprimento de Exigência, a Anvisa irá verificar o atendimento aos requisitos da Resolução – RDC nº 359/2020.
| Petição | Resultado da Análise | Manifestação |
|---|---|---|
|
DIFA
(Solicitação de CADIFA ou Petição de Mudança) |
||
| Deferimento |
CADIFA*
/ Ofício de Deferimento |
|
| Exigência | NOtificação de Exigência | |
| Indeferimento | Ofício de Indeferimento | |
| *nova ou revisada | ||
Todos os documentos serão eletrônicos e enviados para a caixa postal da empresa acessível no sistema de peticionamento. A Anvisa não emitirá documentos impressos em papel.
1. DEFERIMENTO
Se o DIFA estiver de acordo com a Resolução – RDC nº 359/2020, de forma a garantir que há o adequado controle do IFA, será concedida ou revisada a CADIFA ou será enviado um Ofício de Deferimento. As mudanças que forem deferidas só irão promover uma revisão da CADIFA, se foram maiores ou alterarem o seu conteúdo.
A ANVISA será encaminhará a CADIFA somente ao seu detentor.
2. EXIGÊNCIA
As petições não são deferidas enquanto as informações que compõem o DIFA não forem satisfatórias. A Anvisa, quando entender necessário, poderá solicitar informações ou esclarecimentos ao detentor do DIFA por meio de Notificação de Exigência. O detentor do DIFA tem 120 dias corridos da leitura da Notificação de Exigência para peticionar o Cumprimento de Exigência ou a solicitação será indeferida. O usual é que ocorra apenas uma rodada de questionamentos, uma segunda seria exceção.
3. INDEFERIMENTO
Se o peticionamento não estiver instruído com a documentação exigida pela Resolução – RDC nº 359/2020, a petição será indeferida na avaliação preliminar sem análise adicional (não administrativa). O não cumprimento da exigência acarretará o indeferimento da petição. Se, após uma ou duas rodadas de exigência, o peticionamento não atender aos requisitos da Resolução – RDC nº 359/2020, a solicitação também será indeferida.
Para as petições de mudança, a versão atual da CADIFA (sem as mudanças solicitadas) permanece válida.
Em todos os casos, a Anvisa enviará um Ofício de Indeferimento com os motivos do indeferimento. No entanto, quando de um novo peticionamento de solicitação de CADIFA para o mesmo IFA ou da mesma mudança, espera-se que todos os motivos do indeferimento tenham sido atendidos no novo peticionamento.
4. DESISTÊNCIA
O detentor do DIFA pode solicitar a desistência de qualquer peticionamento, caso a Anvisa ainda não tenha concluído a análise. As petições que tiverem solicitadas a sua desistência terão a situação alterada para “desistência a pedido” e será enviado ao detentor o Ofício de Desistência.
VI. REFERÊNCIAS
- ANVISA. Resolução de Diretoria Colegiada – RDC nº 359, de 27 de março de 2020. 01/04/2020.
- ANVISA. Resolução de Diretoria Colegiada – RDC nº 200, de 26 de dezembro de 2017. 29/01/2018.
- ANVISA. Resolução de Diretoria Colegiada – RDC n° 73, de 7 de abril de 2016. 11/04/2016.
- ANVISA. GUIA nº 24, versão 1. 14/08/2019.
- ICH. ICH M4(R3). 13/01/2004.
- ICH. ICH M4Q(R1). 12/09/2002.
- ANVISA. Resolução de Diretoria Colegiada – RDC nº 222, de 28 de dezembro de 2006. 29/12/2006.
- ANVISA. Resolução de Diretoria Colegiada – RDC nº 204, de 06 de julho de 2005. 07/07/2005.
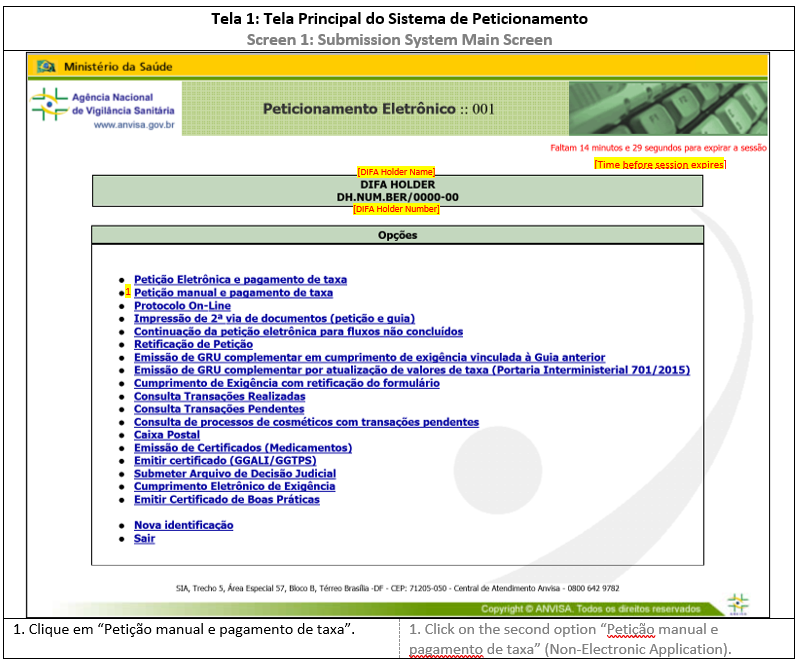
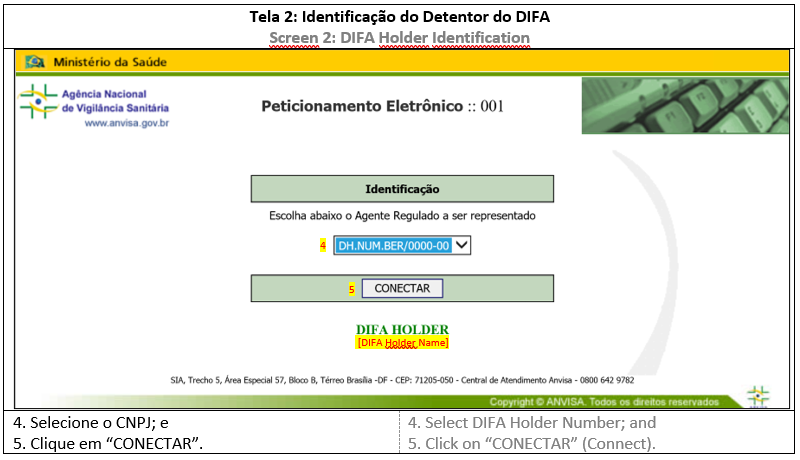
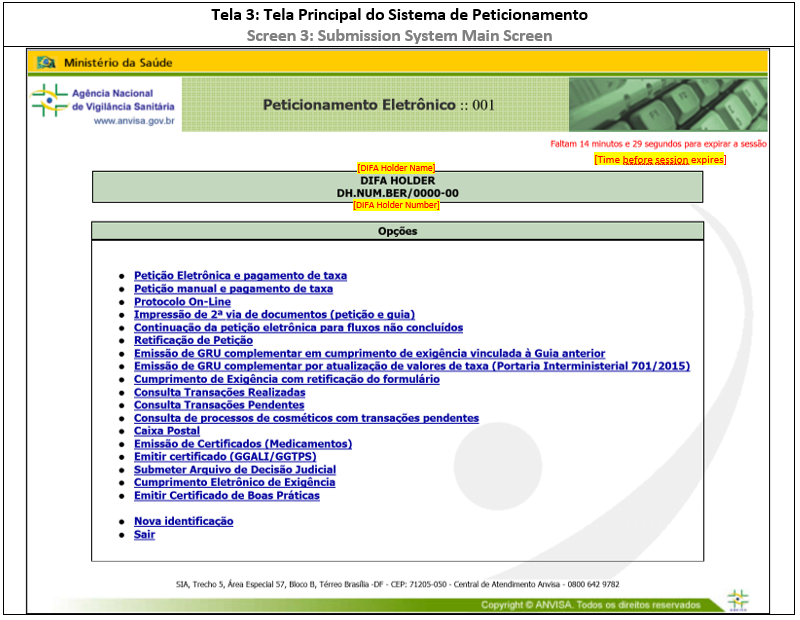
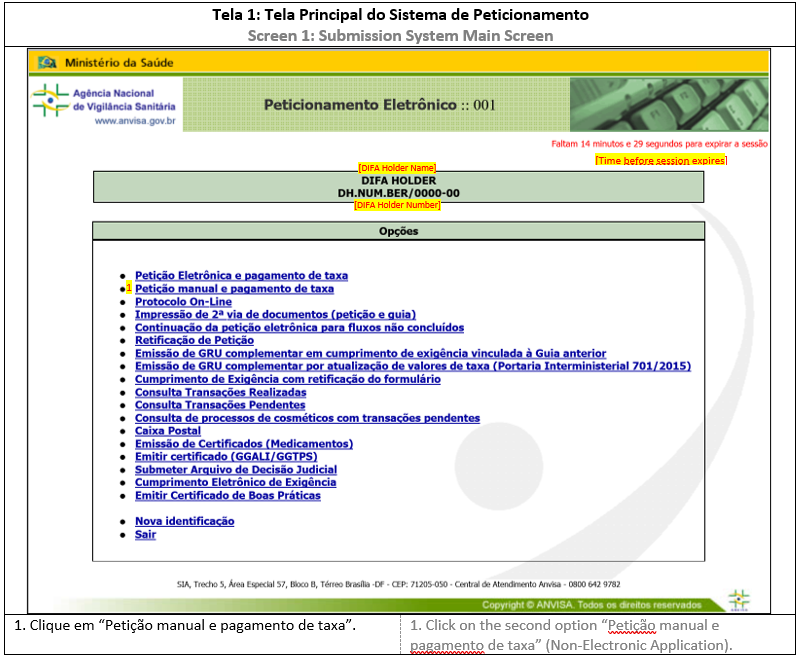
ANEXO 1: COMO ACESSAR O SISTEMA DE SUBMISSÃO
ANEXO 2: PETIÇÃO PRIMÁRIA (PROTOCOLO MANUAL)
ANEXO 3: PETIÇÃO PRIMÁRIA (PROTOCOLO ELETRÔNICO)
ANEXO 4: PETIÇÃO DE MUDANÇA E OUTRAS (PROTOCOLO MANUAL)
ANEXO 5: PETIÇÃO DE MUDANÇA E OUTRAS (PROTOCOLO ELETRÔNICO)
ANEXO 6: CONTINUAÇÃO DE PETIÇÃO NÃO CONCLUÍDA
ANEXO 7: REIMPRESSÃO DE COMPROVANTE DE PROTOCOLIZAÇÃO ON-LINE
ANEXO 8: COMO ACESSAR O SOLICITA
ANEXO 9: PROTOCOLO DE CUMPRIMENTO DE EXIGÊNCIA
ANEXO 10: ACESSANDO CAIXA POSTAL E LENDO MENSAGEM
ANEXO 11: CONSULTA À SITUAÇÃO DE DOCUMENTOS
ANEXO 12: ACOMPANHANDO A SITUAÇÃO DE DOCUMENTOS